【新規参入】医療機器製造販売業許可の取得要件とは?元・総責の行政書士が解説

「アイデアと技術があるので、医療機器メーカーとして挑戦したい。でも法律の壁が、、、」
そんなお悩みを抱えていませんか?
医薬品医療機器等法(薬機法)は非常に難解なので一歩踏み出すのに躊躇してしまいますよね。
実は、医療機器製造販売業許可の最大の壁は、書類の多さではなく「適切な人材と体制の確保」にあります。
本記事では、医療機器メーカーで総括製造販売責任者として現場で監査対応も経験してきた行政書士が、実務経験に基づいた「最短で許可を得るための3つのポイント」を分かりやすく解説します。
この記事でわかること
- 医療機器製造販売業許可の概要
- 医療機器製造販売業許可の取得ポイント
- 総括製造販売責任者の要件
- QMS /GVP体制の構築
- 手順書・記録の作成
医療機器製造販売業許可とは?
医療機器製造販売業許可とは、製品を市場に流通させ、その品質、有効性と安全に最終責任を持つ事業者のための許可です。
名前は「製造」とついていますが、実際に工場でモノを作ることはできませんが
メーカーとして、いわゆる薬事申請を行うのは製造販売業者です。
「製品の企画」「品質管理」「市場への出荷判定」、健康被害などのトラブルが起きた際の「回収対応」などを行います。
製造販売業と製造業の違い
製造販売業と製造業は名前が似ているので混乱してしまう方も多いと思います。
少々荒い表現ですが、「製造販売=元請け(責任者)」、「製造=下請け(工場)」と捉えるとイメージしやすいと思います。
医療機器製造販売業許可を取るためのポイントを解説
まずは総括製造販売責任者の確保から
医療機器の製造販売業許可を取るには、「総括製造販売責任者」の設置が必須です。
まずは要件を満たす人の確保から進めてください。
総括製造販売責任者になるには、学歴や実務経験、講習会の受講などの方法があります。
| 項目 | 高度管理医療機器/管理医療機器 | 一般医療機器 |
|---|---|---|
| 学歴 | 大学等で物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学の専門課程を修了 | 高校等で物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学の専門課程を修了 |
| 学歴 + 実務経験 | 高校等で物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学の専門課程を修了後、医薬品、医療機器又は再生医療等製品の品質管理又は製造販売後安全管理に関する業務に3年以上従事 | 高校等で物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学の科目を修了後、医薬品、医療機器又は再生医療等製品の品質管理又は製造販売後安全管理に関する業務に3年以上従事 |
| 実務経験 + 講習 | 医薬品、医療機器又は再生医療等製品の品質管理又は製造販売後安全管理に関する業務に5年以上従事した後、別に専門の講習を修了した者 |
総括製造販売責任者とは?
製品の品質管理や製造販売後(市場に出した後)の安全管理を行う責任者です。
経営層から法令違反の疑いがある指示が出されたような時は、意見を発して適法に進むよう軌道修正させる責務をがあります。
体制を構築する(QMS /GVP)
医療機器製造販売業には、品質管理の体制(QMS1)と製造販売後安全管理の体制(GVP2)の構築が要求されます。
命や健康に大きく関わる医療機器は、品質管理や安全管理の体制が重視されています。
責任者を置く
下図のような、総括製造販売責任者をトップとする品質保証を確保する責任者を配置します。
ここでは、最も数が多い第二種医療機器製造販売業者について記載しています。
| 責任者 | 要件 | 主な業務 |
|---|---|---|
| 国内品質業務運営責任者 | ・製造販売業者における品質保証部門の責任者 ・品質管理業務等の業務経験が3年以上ある者 ・品質管理業務を適正かつ円滑に遂行できる能力があること ・医療機器等の販売に関する部門に所属していないこと | ・品質管理業務を統括 ・品質管理業務の適正かつ円滑な実施を確認し、記録を作成し保存する ・国内に流通させる製品の市場出荷の決定 ・品質情報の収集/総責への報告 ・回収にかかる回収品の管理および記録の作成/総責への報告 ・製造業者の監督 |
| 安全管理責任者 | ・安全確保業務を適正かつ円滑に遂行できる能力があること ・医療機器等の販売に関する部門に所属していないこと | ・安全確保業務を統括 ・安全確保業務の適正かつ円滑な実施を確認し、記録を作成し保存する ・安全確保業務について必要がある場合は総責に文書で意見を述べ、写しを保存する ・安全管理情報の収集 ・安全確保措置の立案・実施/総責への報告 |
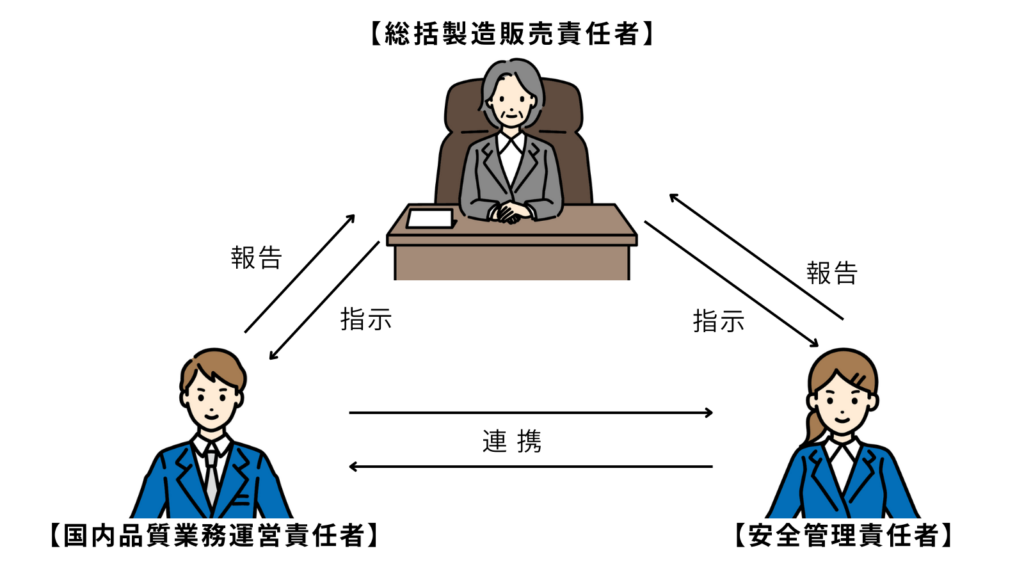
総括製造販売責任者・国内品質業務運営責任者・安全管理責任者は、条件によって兼務が可能です。
手順、記録の作成
品質管理と製造販売後安全管理に係る手順書(マニュアル)の作成が必要です。
それぞれ「QMS省令」「GVP省令」への準拠が求められます。
「手順書を作るだけならなんとかなる」と思われがちですが、QMS/GVPの手順書は数十種類に及び、整合性を取るだけでも膨大な時間がかかります。
さらに、実際の行政による実地調査では『手順書通りに記録が残されているか』を厳しくチェックされます。 当事務所では、現場経験を活かし「実務で回せる、無理のない手順書作成」をサポートします。
まとめ
医療機器製造販売業許可の取得には、要件を満たす責任者(人)の確保と、QMS/GVP(体制)の構築が必須です。 これらをゼロから自社だけで整備するには、半年〜1年以上の時間がかかることも珍しくありません。
「自社の製品はどの区分になる?」「誰が責任者になれる?」など、疑問点があればまずはお気軽にご相談ください。
現場を知る行政書士が、事業化までの道のりを並走します。
\ 初回相談は無料です /












コメント